Pracownia Podstaw Biofizyki/PPB2a
Identyfikacja i ocena stężenia wybranych związków organicznych na podstawie widm w podczerwieni. dr Beata Wielgus-Kutrowska
Spis treści
Wstęp
Podczerwienią (odkrytą w 1800 roku przez Wiliama Herschela) nazywamy umownie zakres promieniowania elektromagnetycznego znajdujący się pomiędzy światłem widzialnym a mikrofalami i obejmujący długości fali w od 780 nm do 1 mm. Ten obszar dzieli się zwyczajowo na następujące pasma:
- bliska podczerwień (ang. near infrared, NIR), 0,7-5 μm),
- średnia podczerwień (ang. mid infrared, MIR), 5-30 μm),
- daleka podczerwień (ang. far infrared, FIR), 30-1000 μm).
W zakresie NIR obserwuje się widma cząsteczek chemicznych mające bezpośredni związek z ich budową, dlatego też metoda badawcza oparta na analizie widm w podczerwieni jest stosowana do badania struktur cząsteczek i ich zanieczyszczeń, a spektroskopia podczerwieni jest rutynowo wykorzystywana w laboratoriach naukowych i przemysłowych.
Cel ćwiczenia:
- Zapoznanie się z metoda badawczą opartą na spektroskopii podczerwieni,
- poznanie zasady działania spektrometru podczerwieni z transformata Fouriera (FTIR) oraz zasad pracy z materiałami stosowanymi w pracy,
- przeprowadzenie typowego eksperymentu polegającego na rejestracji widm w podczerwieni ,
- analiza widm uzyskanych w trakcie wykonywania ćwiczenia.
Podstawowe pojęcia
Promieniowanie elektromagnetyczne składa się z fal o zmieniających się na przemian natężeniach pól elektrycznego i magnetycznego. Fale te rozprzestrzeniają się z prędkością światła i odznaczają się określoną energią, długością i częstotliwością. Długość fali jest związana z częstotliwością zależnością:
- [math]\nu=\nicefrac c\lambda\;\;[/math],
a z energią:
- [math]E=\nicefrac{hc}\lambda\;\;[/math],
gdzie: [math]\lambda\;\;[/math] — długość fali, [math]c\;\;[/math] — prędkość światła, [math]h\;\;[/math] — stała Plancka, [math]\nu\;\;[/math] — częstotliwość, [math]E\;\;[/math] — energia.
Zdefiniowano liczbę falową jako odwrotność częstotliwości i oznaczono jako:
- [math]\tilde{\nu}=\nicefrac 1\nu\;\;[/math].
Energia promieniowania elektromagnetycznego może być absorbowana lub emitowana przez atomy, które przechodzą wtedy na inny poziom energetyczny. Ta absorbowana lub emitowana porcja energii nie może mieć dowolnej wartości, musi odpowiadać przerwie między poziomami energetycznymi atomu z którym oddziałuje — jest skwantowana.
Na całkowitą energię cząsteczki składa się energia ruchu translacyjnego, obrotowego, oscylacyjnego i energia elektronowa, [math](E_\text{czasteczkowa}= E_\text{el}+ E_\text{osc}+ E_\text{rot}+ E_\text{trans})\;\;[/math], a absorpcja lub emisja promieniowanie prowadzi do zmiany stanu energetycznego. I tak zaabsorbowanie kwantu energii w zakresie mikrofal prowadzi do zmiany energii rotacyjnej, w zakresie podczerwieni powoduje zmianę stanu oscylacyjnego, a absorbcja promieniowania widzialnego lub nadfioletu prowadzi do zmian energetycznych stanów elektronowych cząsteczek.
Jak wspomniano przejścia między stanami rotacyjnymi można badać w zakresie mikrofal. Obserwacja w podczerwieni przejść między stanami rotacyjnymi jest możliwa dzięki sprzężeniu rotacji z oscylacjami. Stany energetyczne odpowiadające rotacjom cząsteczek rejestruje się tylko w fazie gazowej. W cieczy jest to niemożliwe, ze względu na częste zderzenia cząsteczek, a w związku z tym niemożność wykonywania przez nie pełnych obrotów[1]. Rejestracja widm oscylacyjnych jest natomiast możliwa dla substancji w stanie ciekłym i stałym.
Oscylacje makromolekuł
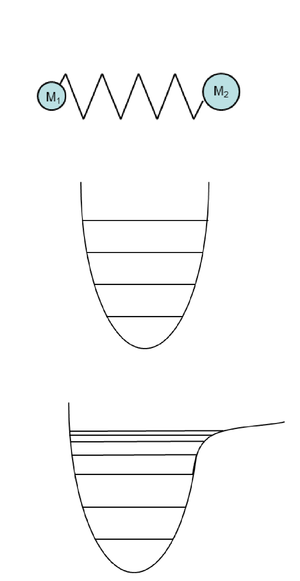
Rozważając model klasyczny drgającej cząsteczki dwuatomowej w potencjale harmonicznym traktujemy ją jako układ dwóch mas połączonych sprężyną. Mogą one wykonywać oscylacje, których częstotliwość zależy od masy zredukowanej układu [math]m_\text{red}\;\;[/math] i stałej siłowej [math]k\;\;[/math], zgodnie z zależnością:
- [math]\nu =\frac{1}{2\pi}\sqrt{\frac k {m_\text{red}}}\;\;[/math].
W przypadku modelu kwantowego energia cząsteczki może przyjmować tylko określone wartości: [math]E_n = \left(n+\frac{1}{2}\right) h\nu\;\;[/math], które determinuje reguła wyboru Δn=±1. Cząsteczka może pochłaniać lub emitować energię równą [math]h\nu\;\;[/math].
Realne cząsteczki są opisywane za pomocą oscylatora anharmonicznego, opisanego zależnością:
- [math]E_n =h\nu_0 \left(n+\frac{1}{2}\right)-h\nu_0 x\left(n+\frac{1}{2}\right)^2\;\;[/math],
dla którego w przypadku drgań o niskiej energii można stosować przybliżenie potencjału harmonicznego, natomiast dla wyższych energii przybliżenie to przestaje obowiązywać.
Reguła wyboru umożliwia pojawienie się słabszych nadtonów [math]\Delta n=\pm2,3\ldots\;\;[/math] odpowiadających przejściom [math]\Delta E=\pm2h \nu, 3h\nu\;\;[/math]. W przypadku skrajnie wysokich energii dochodzi do dysocjacji cząsteczki.
Rodzaje drgań oscylacyjnych i częstości grupowe
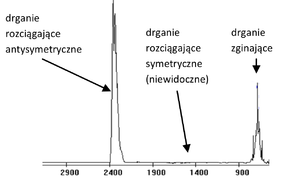
Oscylujące cząsteczki wykonują drgania rozciągające, którym towarzyszy zmiana długości wiązania i deformacyjne (zginające). Nawet najbardziej z pozoru skomplikowane drgania można rozłożyć na tak zwane drgania własne, np. cząsteczka H2O ma trzy drgania własne: zginające, rozciągające symetryczne i rozciągające antysymetryczne. Wszystkie nieliniowe cząsteczki zawierające [math]N\;\;[/math] atomów posiadają [math]3N-6\;\;[/math] a liniowe [math]3N-5\;\;[/math] drgań własnych. Każdemu z tych drgań odpowiada pewna krzywa potencjału i zbiór poziomów energetycznych. Aby cząsteczka mogła drgać musi pochłonąć kwant energii, odpowiadającej pasmom absorpcyjnym widocznym w widmie podczerwieni.
Jednak są tu widoczne tylko drgania związane ze zmianą momentu dipolowego cząsteczki. W związku z tym nie wszystkie mody drgań są widoczne w podczerwieni. Na przykład liniowa cząsteczka CO2 ma 4 drgania własne, natomiast w widmie widać dwa pasma ponieważ jedno z drgań jest zdegenerowane, a jedno nie jest aktywne w podczerwieni.
Dla wieloatomowych cząsteczek trudno jest analizować każdy mod drgań całej cząsteczki. Zakłada się, że każda grupa funkcyjna w cząsteczce może by analizowana niezależnie, np. -CH3 ma te same drgania niezależnie gdzie jest dołączona. Każda grupa funkcyjna, których przykładem jest -CH3 posiada zbiór częstości grupowych odpowiadających drganiom własnym grupy. Na Rys. Figure 4 pokazane są przykładowe grupy funkcyjne oraz zakresy widma podczerwieni, w których należy szukać drgań związanych z obecnością w cząsteczkach tych grup funkcyjnych.
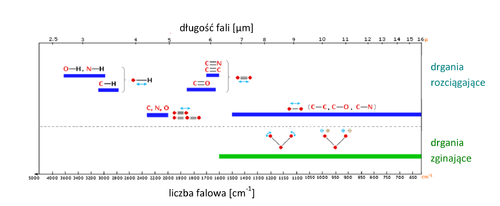
Częstotliwości drgań grup funkcyjnych podlegają pewnym regułom. I tak:
- Drgania rozciągające mają wyższe częstotliwości niż odpowiadające im drgania zginające.
- Wiązanie z wodorem ma wyższą częstotliwość drgań rozciągających niż analogiczne wiązanie z cięższym atomem.
- Wiązania potrójne mają wyższe częstotliwości drgań rozciągających niż odpowiednie wiązania podwójne a te mają wyższe częstotliwości niż odpowiadające im drgania pojedyncze (za wyjątkiem wiązania z wodorem).
- Znajomość stabelaryzowanych drgań grupowych umożliwia identyfikacje cząsteczek chemicznych oraz ich zanieczyszczeń poprzez badanie widm podczerwieni.
Prawo Lamberta-Beera
Intensywność promieniowania przechodzącego przez absorbujący ośrodek ulega osłabieniu zgodnie ze wzorem:
- [math]I=I_0 e^{-\varepsilon c l}\;\;[/math],
gdzie: [math]I_0\;\;[/math] — natężenie wiązki promieniowania padającego, [math]I\;\;[/math] — natężenie wiązki promieniowania po przejściu przez roztwór absorbujący, [math]l\;\;[/math] — grubość warstwy roztworu, [math]c\;\;[/math] — stężenie substancji absorbującej, [math]\varepsilon\;\;[/math] — współczynnik absorpcji.
Definiujemy transmitancję jako:
- [math]T=\frac{I_0}I\;\;[/math],
a absorbancję jako:
- [math]A=-\ln T = -\varepsilon \cdot c \cdot l\;\;[/math].
Stąd, mierząc na pomocą spektrofotometru podczerwieni transmitancję próbki możemy obliczyć absorbancję, która dla ustalonej grubości warstwy absorbującej będzie zależała liniowo od stężenia tej substancji. Znając wartość współczynnika absorpcji i długość drogi optycznej można w ten sposób wyznaczyć stężenie substancji absorbującej.
Ponieważ absorbancja zależy w sposób liniowy od stężenia przy ustalonej długości drogi optycznej, wykreślając krzywą kalibracyjną [math]A(c)\;\;[/math] dla znanych stężeń substancji, można ocenić zawartość tej substancji w próbce o nieznanym stężeniu.
Technika pomiaru
Urządzenie, które zostanie wykorzystane w pomiarach to spektrofotometr podczerwieni z transformatą fourierowską (FTIR). W przypadku tradycyjnych pomiarów próbkę oświetla się wiązką promieniowania o zmieniającej się częstotliwości. Czas pomiaru to 10-100 min. W technice pomiarowej opartej na transformacji Fouriera na substancje pada wiązka polichromatyczna obejmująca cały zakres interesujących nas częstości.
Widma nie obserwuje się bezpośrednio, ale mierzy się sygnał w funkcji czasu a następnie dokonuje transformacji przekształcając zależność [math]y(t)\;\;[/math] w zależność [math]x(v)\;\;[/math]. Pozwala to na znaczne skrócenie czasu pojedynczego pomiaru (sekundy). Rejestrację można powtarzać i uśredniać sygnał, co poprawia stosunek N/S.
Pomiary w zakresie podczerwieni wymagają kuwet o okienkach przepuszczających promieniowanie w tym zakresie. Odpowiednimi substancjami są sole, KBr, NaCl, CaF2 i inne. Jak wiadomo woda rozpuszcza sole takie jak NaCl, KBr, dlatego w przypadku pracy z kuwetami wykonanymi z tego typu materiałów należy stosować rozpuszczalniki nie zawierające wody i pracować w warunkach uniemożliwiających kontakt kuwet z wilgocią. Uwaga ta dotyczy również spektrofotometru gdyż pryzmaty optyczne są zwykle wykonane z bromku potasu. Jako rozpuszczalniki zwykle stosuje się wtedy chloroform, deuterowany chloroform, CCl4 itp. Kuwety z fluorku wapnia nie rozpuszczają się w wodzie.
Warunki przystąpienia do części eksperymentalnej ćwiczenia
Warunkiem przystąpienia do części eksperymentalnej jest zaliczenie kolokwium wstępnego. Wybór sposobu przeprowadzenia kolokwium wstępnego należy do prowadzącego ćwiczenie. Materiał z zakresu spektroskopii podczerwieni obowiązujący w czasie kolokwium wstępnego i wykonywania części eksperymentalnej ćwiczenia został przedstawiony w niniejszej instrukcji, oraz w umieszczonej na końcu instrukcji bibliografii. W szczególności należy przeczytać odpowiednie rozdziały z książki Z. Kęckiego, Podstawy spektroskopii molekularnej oraz G. Barrowa Wstęp do spektroskopii molekularnej.
Zagadnienia, które mogą pojawić się na kolokwium wstępnym:
- Podstawowe pojęcia związane z promieniowaniem elektromagnetycznym i pomiarami spektroskopowymi: długość fali, częstość drgań, liczba falowa, stan podstawowy, stan wzbudzony, zakres promieniowania podczerwonego. Rodzaje energii molekuł, kwantowanie energii.
- Pomiar absorpcji i emisji promieniowania elektromagnetycznego. Schematyczne przedstawienie zasady pomiarów absorpcji i emisji. Co oznaczają pojęcia „widmo absorpcyjne” i „widmo emisyjne”?
- Wygląd absorpcyjnego widma rotacyjnego cząsteczki dwuatomowej. W jakim zakresie promieniowania obserwuje się absorpcyjne pasma rotacyjne? Schemat poziomów energetycznych i przejść energetycznych dozwolonych przez reguły wyboru.
- Fizyczny opis oscylacji molekuł. Jakie rodzaje drgań mogą wykonywać molekuły. Które z nich są widoczne w podczerwieni? Interpretacja widma oscylacyjnego.
- Co to jest widmo oscylacyjno-rotacyjne cząsteczki dwuatomowej? W jakim zakresie promieniowania obserwuje się absorpcyjne pasma oscylacyjne? Schemat poziomów energetycznych i przejść energetycznych dozwolonych przez reguły wyboru Wygląd widma absorpcyjnego, związek ze strukturą i obsadzeniem poziomów energetycznych Czym się różni równoległe pasmo absorpcyjne od prostopadłego pasma absorpcyjnego? Badania, w których wykorzystuje się widma oscylacyjno-rotacyjne molekuł.
- Aparatura. Problemy materiałowe (przepuszczanie podczerwieni), spektrofotometry IR klasyczne i z transformatą Fouriera (FT).
Wykonanie ćwiczenia
Ćwiczenie będzie polegało na:
- interpretacji widm w podczerwieni wybranych związków chemicznych, np. CH4, CHCl3, CDCl3 i CCl4,
- oznaczeniu zawartości wybranego związku (np. difenyloaminy) w rozpuszczalniku (np. CCl4).
Po zapoznaniu się z zasadami BHP, obowiązującymi w trakcie wykonywania ćwiczenia (część A) studenci wykonują pomiary widm:
- metanu w fazie gazowej (próbka nr 1),
- wybranych próbek o nieznanej zawartości (próbki nr 2, 3 i 4).
W widmie metanu należy zidentyfikować pasmo (pasma) związane z drganiami grupy C-H, omówić jego wygląd, zwracając uwagę na występowanie metanu w fazie gazowej, a następnie określić jakie substancje (CHCl3, CDCl3 i CCl4) znajdują się w kolejnych próbkach.
W części B ćwiczenia należy przygotować roztwory (10%, 20%, 30% i 40%) dwumetyloaminy lub chloroformu w czterochlorku węgla, zarejestrować ich widma w podczerwieni i wykreślić krzywą kalibracyjną dla wybranej liczby falowej.
Po otrzymaniu od asystenta roztworów o nieznanym stężeniu tych związków należy określić ich stężenie.
Opis ćwiczenia
W opisie w części A powinna się znaleźć interpretacja uzyskanych widm oraz identyfikacja badanych związków.
W części B należy na podstawie krzywej kalibracyjnej ocenić zawartość badanej substancji w rozpuszczalniku.
Literatura
- Z. Kęcki, Podstawy spektroskopii molekularnej
- G. Barrow, Wstęp do spektroskopii molekularnej
- Metody spektroskopowe i ich zastosowanie do identyfikacji związków organicznych — praca zbiorowa pod redakcją Wojciecha Zielińskiego i Andrzeja Rajcy
- J. A. Barltrop i J. D. Coyle, Fotochemia, podstawy
- J. Simons, Fotochemia i spektroskopia
- L. A. Kazicyna i N. B. Kupletska, Metody spektroskopowe wyznaczania struktury związków organicznych
- K. Butkiewicz (tłumacz), Ćwiczenia laboratoryjne z chemii fizycznej
- L. Sobczyk, A. Kisza i K. Gatner, Eksperymentalna chemia fizyczna
- ↑ Dokładniejsze, wymagane na kolokwium wstępnym informacje dotyczące widm rotacyjnych cząsteczek znajdą Państwo w polecanej literaturze, w tym w podręcznikach: Z. Kęcki, Podstawy spektroskopii molekularnej oraz G. Barrow, Wstęp do spektroskopii molekularnej.